Sáng nay 26/6, Thủ tướng Chính phủ Phạm Minh Chính dẫn đầu đoàn công tác làm việc với TPHCM. Sau khi kiểm tra công tác phòng chống dịch COVID-19 tại Khu cách ly tập trung Ký túc xá ĐHQG TPHCM, Thủ tướng cùng đoàn đã đến làm việc với Công ty Nanogen, một trong 4 đơn vị sản xuất vắc xin ở nước ta.
 |
Thủ tướng Phạm Minh Chính làm việc với Công ty Nanogen vào sáng 26/6- ảnh H.L |
Tại buổi làm việc, ông Hồ Nhân- Tổng giám đốc Công ty Nanogen cho biết hiện công ty đã gửi mẫu vắc xin NanoCovax cho WHO để tổ chức này kiểm tra và thẩm định chất lượng. “Đến thời điểm này, NanoCovax đã bước sang giai đoạn 3 của thử nghiệm. Chúng tôi đã thử nghiệm trên 1000 ứng viên ở miền Bắc và miền Nam, trong 10 ngày tới sẽ đẩy nhanh thử nghiệm cho 12 nghìn người còn lại. Dự kiến tháng 7 tới sẽ chuyển sang giai đoạn 3C tiêm trên 1 triệu người ở cả nước”- ông Hồ Nhân cho biết.
 |
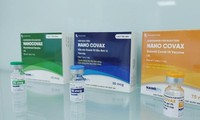
| Bên trong nhà máy sản xuất vắc xin NanoCovax của công ty Nanogen |
Theo ông Nhân, hiện công ty có 4 nhà máy sản xuất vắc xin với năng lực đáp ứng nhu cầu tiêm chủng cho người dân trong nước. “Ngoài gửi mẫu cho WHO kiểm tra, chúng tôi cũng nhận được sự hợp tác của nhiều nước về phân phối vắc xin NanoCovax sau khi thử nghiệm xong. Trong đó, Ấn Độ đã làm việc và có biên bản ghi nhớ phân phối vắc xin của công ty”- ông Nhân thông tin thêm với đoàn làm việc.
Người đứng đầu Nanogen cho biết dựa trên các kết quả thử nghiệm lâm sàng, khả năng sinh miễn dịch của vắc xin Nanocovax cho thấy vắc xin đạt 99,4%, so sánh với các loại vắc xin khác trên thế giới là không hề thua kém và có phần cao hơn. Công suất sản xuất hiện nay của nhà máy Nanogen đạt 8-12 triệu liều/tháng và đến tháng 12/2021 sẽ sản xuất 50 triệu liều tiêm cho người dân với giá bán dự kiến 120.000 đồng/liều.
Kết thúc báo cáo, ông Hồ Nhân mong muốn Thủ tướng Phạm Minh Chính và Bộ trưởng Y tế Nguyễn Thanh Long sâu sát hơn nữa đến doanh nghiệp sản xuất vắc xin đồng thời mong Bộ Y tế đồng hành cùng đơn vị bằng cách cử một đội chuyên hành động lo về vấn đề sản xuất vắc xin trong nước để tháo gỡ kịp thời khó khăn.
 |
Vắc xin "made in Vietnam" đang thử nghiệm giai đoạn cuối với thông tin tính sinh miễn dịch rất tốt |
Bộ trưởng Y tế Nguyễn Thanh Long cho rằng hiện thế giới có khoảng 130 vắc xin làm theo công nghệ của Nanogen và cũng đang thử nghiệm lâm sàng. “Quan điểm của Bộ Y tế là tạo điều kiện tối đa để thúc đẩy quá trình thử nghiệm nhưng phải đảm bảo an toàn sức khoẻ của người dân”- Bộ trưởng Y tế nói.
Thủ tướng Phạm Minh Chính đánh giá cao công nghệ sản xuất vắc xin của Nanogen và sự kịp thời của công ty khi bắt tay sản xuất vắc xin từ sớm. Tuy nhiên, Thủ tướng cũng đề nghị công ty cần làm rõ một số vấn đề về công nghệ áp dụng, nguyên liệu đầu vào và so sánh chất lượng với các loại vắc xin khác, khả năng sản xuất và giá cả.
 |
Theo ông Hồ Nhân giá dự kiến của vắc xin NanoCovax sẽ khoảng 120 nghìn đồng/ liều |
Trước đó, ngày 15/6, Công ty CP Công nghệ Sinh học Dược Nanogen đã có văn bản gửi Thủ Tướng Chính Phủ xin cấp phép khẩn cấp cho vắc xin Nanocovax do công ty này nghiên cứu. Theo Nanogen, trong tình hình dịch bệnh đang cản trở sự phát triển kinh tế, Nanogen đã nghiên cứu và sản xuất vắc xin Nanocovax phòng COVID-19. Vắc xin đã chứng minh được những thành công bước đầu, dựa trên các kết quả báo cáo giữa kỳ của thử nghiệm lâm sàng giai đoạn 1 và giai đoạn 2 đã được Hội đồng đạo đức trong nghiên cứu y sinh chấp thuận và đánh giá tốt.
Đồng thời, Bộ Y tế và Hội đồng đã thông qua đề cương nghiên cứu, triển khai thử nghiệm lâm sàng giai đoạn 3 cho Nanocovax hàm lượng 25mcg/mL trên quy mô 13.000 người. Dựa trên các kết quả thử nghiệm lâm sàng, khả năng sinh miễn dịch của vắc xin Nanocovax đạt 99,4%. Tuy nhiên, đại diện Bộ Y ế cho rằng vắc xin NanoCovax nghiên cứu dù có tính sinh miễn dịch tốt nhưng chưa đủ cấp phép khẩn cấp.
Bởi, vắc xin còn trong quá trình nghiên cứu, thử nghiệm, chưa xong và chưa có dữ liệu. Hiện nay vắc xin NanoCovax mới tiêm thử nghiệm mũi thứ nhất của giai đoạn 3 trên 1.000 người. Theo ông Quang, kế hoạch cỡ mẫu giai đoạn 3 thử nghiệm trên 13.000 người. Chưa kể sau tiêm mũi thứ 2 sau 28 ngày, cơ quan chuyên môn cần phải tiếp tục đánh giá sau 36, 45, 56 ngày sau tiêm.